2025年度 三菱電機ソフトウエア技術レポート
多遺伝子パネル検査(MGPT)構築に関する研究
-ゲノム解析技術の発展と臨床応用への展望-
1.はじめに
1953年、ジェームズ・ワトソンとフランシス・クリックらによりDNAの二重らせん構造が発見され、生命科学に革命をもたらした。発見から約50年後の2003年にはヒトゲノム計画(Human Genome Project)が完了した。これによりヒトの全遺伝情報が明らかとなり、疾患関連遺伝子の同定が進められた。しかし、当時はDNAを塩基配列データに変換するシーケンスコスト(1サンプルに対してシーケンスで使用する試薬等の総費用)が極めて高く、研究や臨床での実用化は限定的であった。
2006年頃から次世代シーケンサー(Next Generation Sequencing: NGS)の登場により状況は大きく変化した。また、Roche社、Illumina社、ABI社などによる技術開発競争が進み、シーケンスコストが飛躍的に低下した。例えば、Illumina社であれば、NovaSeqによる大規模解析からNextSeqによる中規模解析まで、目的に応じて選択可能な多様な次世代シーケンサーのプラットフォームを現在整備している。
本稿では、NGS技術の発展とともに普及した多遺伝子パネル検査(Multi-Gene Panel Test: MGPT)に着目し、日本国内での動向、包括的ゲノムプロファイル検査(Comprehensive Genomic Profiling: CGP NGSを活用してがん組織から採取した検体からがんの原因となった遺伝子変異を特定する検査)との相違点、さらに当社でのシステム構築の取組み、今後の課題と展望について報告する。
2.遺伝子検査技術の発展とMGPTの台頭
2007年、米国の23andMe社が一般消費者を対象としたDTC(Direct to Consumer)型の遺伝子検査サービスを開始した。このサービスでは唾液サンプルを郵送するだけでSNP(Single Nucleotide Polymorphism)マイクロアレイ解析を実施し、疾患リスク、薬物反応性、保因者情報、祖先情報などを提供した。一方で、より臨床的な解析サービスとしてAmbry Genetics社及びInvitae社がMGPTサービスを展開しており、NGS技術を用いて疾患関連遺伝子の包括的な解析を実施している。これらは遺伝カウンセリングを含む医療連携型サービスとして確立されてきた。
当社も2000年代初頭からゲノム解析技術の研究開発を行い、2015年頃から臨床現場で活用可能な検査サービスの実装に取り組んできた。
3.日本におけるゲノム医療の進展
日本では2019年、CGP検査が保険適用となり、がん組織や血液から多数の遺伝子変異を一括解析することが可能となった。これは「標準治療が終了又は存在しない進行固形がん」を対象としており、現在ではがんゲノム情報管理センター(C-CAT)の統計情報から年間約20万人以上が検査を受けていると推定される。その中で、約10%の検査対象者において二次的所見として生殖細胞系列変異が検出されている[1]。
一方、MGPTにおいては2018年にミリアド・ジェネティクス社のBRACAnalysisが乳がん治療のコンパニオン診断として保険適用された。さらに2025年3月、厚生労働省科学研究補助金による平沢班の研究成果として「遺伝性腫瘍症候群に関する多遺伝子パネル検査(MGPT)の手引き」が公表された。この手引きでは、56のがん関連原因遺伝子が掲載され、検査体制や説明文書・同意書モデルの提示など、実用化に向けた包括的指針が示された[2]。これにより、日本国内におけるMGPTサービスの標準化と普及が期待されている。
4.CGPとMGPTの比較
遺伝子異常は大きく生殖細胞系列変異(先天的に保持)と体細胞系列変異(環境要因などにより後天的に発生)に分けられる(図1参照)。
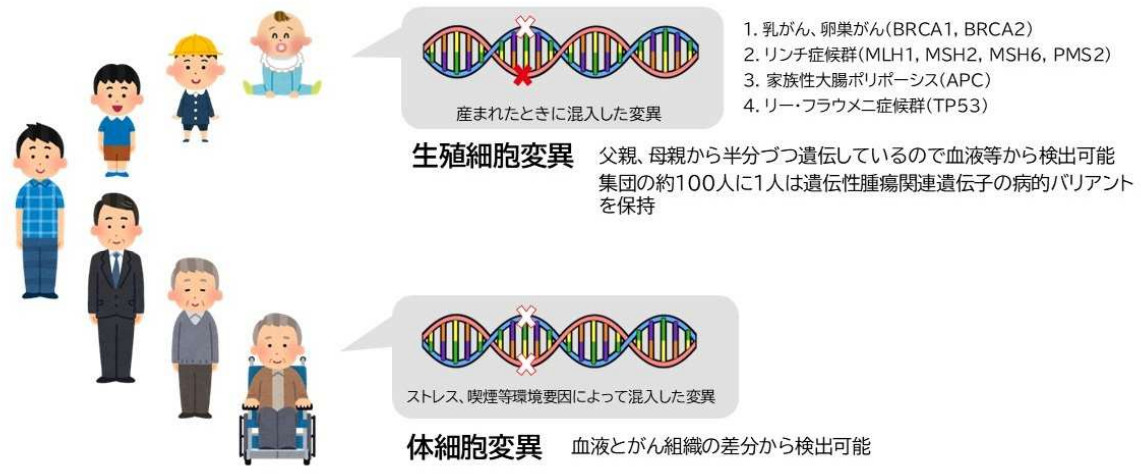
CGPは主に体細胞系列変異を検出し、MGPTは生殖細胞系列変異の特定を目的とする。CGPとMGPTの比較を表1に示す。
| CGP | MGPT | |
|---|---|---|
| 検査組織 | がん組織(FFPE) (+正常組織(血液)) |
正常組織(血液、口腔粘膜) |
| 目的 | 腫瘍の治療方針決定 | 遺伝性がんの診断・リスク評価 |
| 対象者 | がん患者本人 | がん患者本人及びその家族 |
| 検出する遺伝子異常 | SNV(INDEL)、CNV、TMB、MSI、融合遺伝子 | SNV(INDEL)、CNV、モザイク |
| 検出種別 | 体細胞変異 | 生殖細胞系列変異 |
| 使用されるデータベース | COSMIC JAX CKB ClinVar 2KJPN gnomAD |
ClinVar 2KJPN gnomAD |
| 主なサービス | Foundation One NCC OncoGuide GenMineTop |
BRACAnalysis |
- SNV:一塩基置換(Single Nucleotide Variant)
- INDEL:挿入・欠失変異(Insertion/Deletion)
- CNV:コピー数異常(Copy Number Variation)
- TMB:腫瘍遺伝子変異量(Tumor Mutation Burden)
- MSI:マイクロサテライト不安定性(Microsatellite Instability)
- COSMIC(Catalogue of Somatic Mutation in Cancer):Sanger社が管理しているがんゲノムデータベース
- JAX CKB:Genomenon社が管理しているがんゲノムデータベース
- ClinVar:米国NCBIが管理している疾患データベース
- 2KJPN:東北メディカル・メガバンク機構(ToMMo)が管理しているデータベース
- gnomAD:Broad Institute社が管理しているデータベース(Genome Aggregation Database)
両者の主な相違点は次のとおりである。
- ①試料の性質:
CGPではがん組織のFFPE(formalin-fixed paraffin-embedded:ホルマリン固定パラフィン包埋)を使用するが、MGPTは血液や口腔粘膜を使用する。FFPEには正常組織も含まれるため、がん組織の割合が低い場合、検出感度が低下する。 - ②目的:
CGPはがん組織を解析し、腫瘍の治療方針を決定する。一方MGPTは、がん患者の家族を対象としており、遺伝性がんの診断・リスク評価に用いられる。 - ③検出方法:
CGPはがん組織と正常組織を比較し、がん特異的な遺伝子変異を抽出する。一方MGPTは正常組織由来DNAのみを対象とし、個人が持つ遺伝的素因を解析する。 - ④解析手法:
CGPでは、COSMICやJAX CKB等の体細胞の病原性を評価したデータベースを活用し、最終的にはエキスパートパネルが解析結果を臨床的に解釈する。MGPTでは2KJPNやgnomADなどの一般変異データベースを用いて病原性の低い変異を除き、ClinVarなどを用いて病原性の有無を評価する。 - ⑤運用体制:
CGPはがんゲノム医療中核拠点病院で実施され、エキスパートパネルによる多職種協議が行われる。MGPTは一部保険適用されているが、多くは自由診療として実施されている。保険適用が拡大された場合の体制については今後決められていく。
5.当社における取組みとMGPT解析パイプライン
当社では、2015年に「大規模ゲノム解析パイプラインの構築」[3]を行い、これを基盤として「PleSSision Exome検査サービス」を開発した。本サービスは慶應義塾大学病院などの医療機関で提供されており、CGPの臨床実装例として高く評価されている。
当社は、これまでのCGP解析技術を応用し、MGPT解析システムの実用化を通じて社会に貢献していくことを目指している。現在、検討しているMGPT解析システムのパイプラインのワークフローは以下のとおりである。
(1)QCフィルタリング
次世代シーケンサーはDNAを断片化して読み取った塩基配列をリードとして出力する。リード配列にはしばしばアダプター配列や低品質な塩基が混入する。これらをそのまま解析に用いた場合、誤った遺伝子変異の検出につながるおそれがある。そのため、品質管理(Quality Control: QC)工程では、シーケンス時に使用したアダプター配列情報を基にアダプタートリミングを行い、さらに低品質塩基領域のトリミング処理を実施する。これにより、解析に適した高品質リードのみを選別することが可能となる。トリミング後に残存した塩基数をシーケンサーが出力した総塩基数で除算して得られる値をリード残存率と呼び、この指標はサンプル及びシーケンス全体の品質評価に用いられる。
(2)マッピング
NGSによって得られるリードは、ゲノム上の特定領域に対応する短い配列情報である。マッピング工程では、QCフィルタリングにより整理された各リードがゲノム上のどの位置に由来するかをリファレンス配列との比較により決定する。リファレンス配列は国際的な公的データベースにより公開されており、全世界で共通の基準配列が使用されている。
マッピングに用いられる解析ツールでは、リファレンス配列に対して事前にインデックス情報を構築することで、探索効率の大幅な向上を実現している。マッピング後、全リード数に対するマッピングされたリード数の比率を算出した値をマッピング率と呼び、この値はサンプル及びシーケンス全体の品質を示す重要な指標となる。
さらに、解析対象領域においてリードがどの程度均一に分布しているかを評価する指標としてUniformity(カバレージ均一性)がある。Uniformityは、カバレージ(リードの重なり)が一定以上である領域の割合を算出することで求められる。Uniformityが低い場合、シーケンスデータの品質不良や解析不能領域の存在を示唆するため、データの信頼性を確認する上で不可欠な品質管理指標である。
サンプルを用いて平均depth(そのポジションにおいてシーケンスされたリードの数)とUniformityの関係を図2にまとめた。円の周りにMGPTの手引きで規定された遺伝子を整列させ、中央からの距離を各遺伝子のdepthとしてグラフにしている。平均depthが増加するにつれ、全体的な円の大きさが大きくなるが、一部の遺伝子では低いところがある。これらの場所はpoly-Aやリピート配列を含む領域であり、余裕をもってリードを準備することが重要であることがわかる。
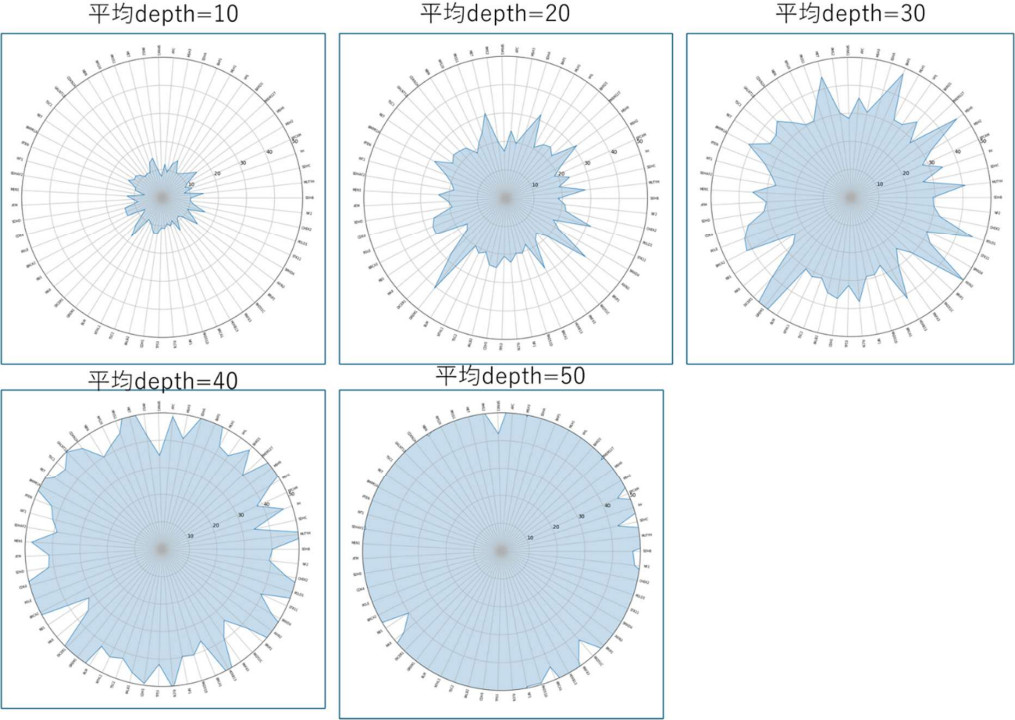
(3)変異検出
リファレンス配列との比較により塩基配列上の差異を抽出し、SNV、INDEL及びCNVを同定する。さらに、カバレージ情報を基に構築されたカバレージデータベースを参照することで、解析対象領域における領域特異的なコピー数変化の検出が可能となる。
(4)アノテーション
検出された遺伝子変異は、ClinVar、gnomADなどの公的データベースを用いてアノテーション(注釈付け)を行い、既報のエビデンスに基づき病原性の有無及び臨床的意義を判定する仕組みを構築した。この際、ClinVarでは病原性の分類基準(pathogenic、likely pathogenic、Variant of Uncertain Significance: VUS、likely benign、benign)が採用されており、これらの評価結果を臨床判断の参考情報として活用する。
さらに、集団特異的な変異評価においては、日本人集団のゲノム多様性を反映した2KJPNデータベースを活用する。2KJPNに蓄積された大規模な日本人リファレンスデータは、海外データベース(gnomADなど)では過小評価される可能性のある日本人特有の遺伝的多様性を補完する役割を果たす。これにより、人種間差異を考慮した精緻で信頼性の高い変異解釈が可能となり、誤検出や誤分類のリスクを低減するとともに、臨床的判断の精度向上に寄与する。
(5)レポーティング
アノテーションによって臨床的意義が付与された変異データの中から、病原性又は病原性の可能性が高い遺伝子変異を抽出し、レポート形式で出力する。このレポートには、各変異のリード率(変異リード数/全リード数)、病原性判定の根拠となる公的データベース情報(ClinVar、2KJPNなど)及び変異アレル頻度(Minor Allele Frequency: MAF)が併記される。これにより、臨床医が変異の信頼性と病的意義を迅速に評価できるよう配慮されている。
一方で、「臨床的意義が不明確」(VUS)な変異については、遺伝カウンセリングの現場での混乱や不安を最小化する観点から、報告対象とするか否かを慎重に判断する必要がある。VUS変異の扱いには、医師・遺伝カウンセラー・臨床検査技師間の情報共有体制が重要であり、倫理的・社会的観点も考慮されるべきである。
さらに、レポートには解析の品質保証指標として、リード残存率、マッピング率、Uniformity、DNA品質、ライブラリ調製効率などを含め、検査過程の再現性と信頼性を担保する。これらの品質情報を併記することで、臨床判断における結果の透明性を高め、医療現場でのデータ活用をより確実なものとすることができる。
6.むすび
がん予防及び早期発見の観点から、MGPTは極めて有効な手段である。2025年の「MGPTの手引き」公表を契機に、日本国内でも保険適用を前提とした体制整備が進むと予測される。一方で、遺伝専門医やカウンセラーの人材不足、データ解釈の標準化、コンパニオン診断との連携など、多くの課題が残されている。しかし、当社がMGPT解析システムを実用化することにより、個々の遺伝情報に基づく精密医療が実現し、より良い生活と持続可能な医療体制の構築が期待される。
最後に、本稿をまとめるにあたり貴重なデータの提供及びご指導いただいた、岡山大学学術研究院医歯学域 平沢晃教授、慶應義塾大学医学部腫瘍センターがんゲノム医療ユニット 西原広史教授、中村康平専任講師及び同ユニットの皆様に深くお礼を申し上げる。
商標
- ・NovaSeq、NextSeqは、illumina社の登録商標である。
- ・BRACAnalysisは、ミリアド・ジェネティクス社の登録商標である。
- ・Foundation Oneは、Foundation Medicine, Incの登録商標である。
- ・OncoGuideは、シスメックス社の登録商標である。
- ・GenMineTOPは、コニカミノルタREAL社の登録商標である。
- ・ToMMoは、東北大学の登録商標である。
- ・JAXは、The Jackson Laboratoryの登録商標である。
- ・PleSSisionは、三菱電機ソフトウエア株式会社の登録商標である。
参考文献
- [1]池田健:当院におけるがん遺伝子パネル検査の実績と展望− がんゲノムから遺伝カウンセリングまで −,道南医学会ジャーナル,8巻,1号,22~26(2025)
- [2]日本遺伝性腫瘍学会/令和6年度厚労科研 がん対策推進総合研究事業 平沢班:遺伝性腫瘍症候群に関する多遺伝子パネル検査(MGPT)の手引き, 金原出版, 2025
- [3]野原祥夫:大規模ゲノム解析パイプラインの構築, MSS技報,vol25,2015